Axit cacboxylic là hợp chất hữu cơ được tìm thấy nhiều trong tự nhiên, ví dụ như axit acetic trong dấm hay axit citric có trong quả chanh... Vậy nó có cấu tạo như thế nào? Tính chất hóa học và tính chất vật lý? Ứng dụng trong đời sống? Chúng ta hãy cùng nhau tìm hiểu thông qua bài viết dưới đây nhé!
1. Axit cacboxylic là gì?
Axit cacboxylic là hợp chất hữu cơ, trong đó nguyên tử cacbon (C) được liên kết với nguyên tử oxy (O) bằng liên kết đôi và với nhóm hydroxyl (―OH) bằng liên kết đơn.
Công thức chung của axit cacboxylic là R−COOH hoặc R−CO2H, với R có thể là nhóm alkyl , alkenyl, aryl hoặc nhóm khác.
2. Danh pháp của axit cacboxylic
Axit cacboxylic thường được xác định bằng tên thông thường. Chúng thường có hậu tố -ic. Ví dụ axit butyric (C3H7COOH) là axit butanoic.
Các phân tử phức tạp chứa axit cacboxylic, cacboxyl có thể được coi là vị trí một trong chuỗi gốc ngay cả khi có các nhóm thế khác như axit 3-chloropropanoic. Ngoài ra, nó có thể được đặt tên là nhóm thế "cacboxy" hoặc "axit cacboxylic" trên cấu trúc gốc khác như 2-cacboxyfuran.
Tuy nhiên hầu hết axit cacboxylic đơn giản có tên thường gọi bởi chúng được phân lập từ các nguồn sinh học. Ví dụ như CH3CH2CH2COOH là axit butyric, lần đầu tiên thu được từ bơ nên được đặt tên theo từ butyrum trong tiếng Latinh có nghĩa là "bơ".
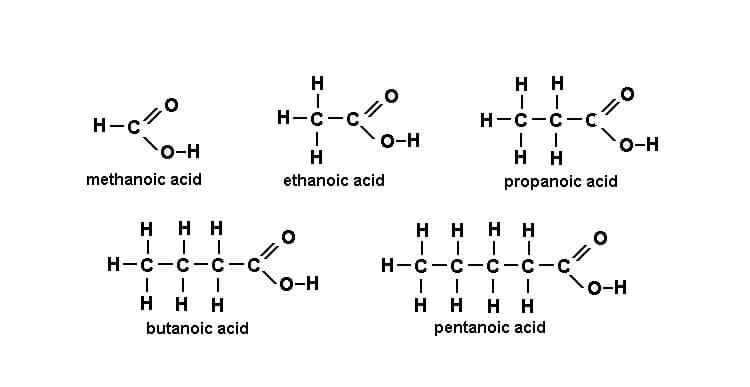
Tên gọi một số axit cacboxylic
3. Phân loại axit cacboxylic
Dựa theo đặc điểm cấu tạo của gốc hiđrocacbon, các axit được chia thành:
- Axit cacboxylic no: Phân tử có gốc ankyl hoặc nguyên tử hiđro liên kết với nhóm -COOH.
Ví dụ như HCOOH; CH3−COOH...
- Axit cacboxylic không no: Phân tử có gốc hiđrocacbon không no, mạch hở gắn với nhóm -COOH.
Ví dụ như CH2=CH−COOH;CH3[CH2]7CH=CH[CH2]7COOH;...
- Axit cacboxylic thơm: Phân tử có gốc hiđrocacbon thơm liên kết với nhóm -COOH.
Ví dụ như C6H5COOH,CH3−C6H4−COOH,...
Ngoài ra, axit cacboxylic còn được phân loại dựa trên số nhóm -COOH:
- Axit cacboxylic đơn chức: Trong phân tử có 1 nhóm - COOH. Ví dụ như HCOOH...
- Axit cacboxylic đa chức: Trong phân tử có hai hay nhiều nhóm -COOH. Ví dụ như axit malonic HOOC−CH2−COOH...
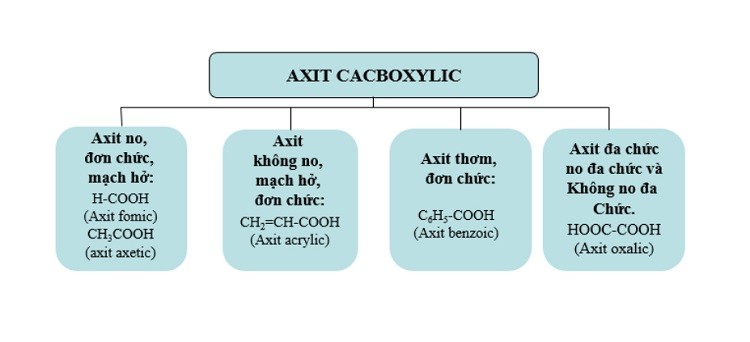
Phân loại axit cacboxylic
4. Tính chất của axit cacboxylic
Các tính chất vật lý và hóa học của acid cacboxylic như sau:
4.1. Tính chất vật lý
- Trạng thái tồn tại: Axit cacboxylic mạch không phân nhánh (axit béo) là chất lỏng ở nhiệt độ phòng.
- Mùi: Axit từ axit propanoic (C3) đến axit decanoic (C10) có mùi rất hôi, khó chịu.
- Độ hòa tan: Độ hòa tan của axit cacboxylic trong nước tương tự như độ hòa tan của rượu, andehit và xeton . Axit có ít hơn khoảng 5 nguyên tử cacbon hòa tan tốt trong nước. Với những chất có trọng lượng phân tử cao hơn thường không hòa tan do phần hydrocacbon lớn hơn kỵ nước. Tuy nhiên, các muối natri, amoni và kali của axit cacboxylic thường hòa tan tốt trong nước.
- Điểm sôi: Axit cacboxylic có nhiệt độ sôi cao hơn nhiều so với hydrocacbon, rượu, ete , andehit hoặc xeton có trọng lượng phân tử tương tự.
>>>XEM THÊM:Mua Ammonium sulfate (NH4)2SO4, Nhật Bản, đóng gói 50kg/bao với giá tốt.
4.2. Tính chất hóa học
- Tính chất hóa học chính của axit cacboxylic là tính axit. Chúng thường có tính axit mạnh hơn các hợp chất hữu cơ khác có chứa các nhóm hydroxyl nhưng thường yếu hơn các axit vô cơ quen thuộc (như axit clohydric HCl, axit sunfuric H2SO4…).
Axit cacboxylic thể hiện tính acid bằng cách phản ứng với bazơ để tạo thành muối cacboxylat, trong đó hydro của nhóm hydroxyl (-OH) được thay thế bằng cation kim loại.
CH3COOH + NaHCO3 → CH3COONa + CO2 + H2O
Ngoài ra, nó còn có thể phản ứng với oxit base, muối carbonat...
- Một số phả ứng khác của axit cacboxylic là:
- Phản ứng este hóa: Đây là phản ứng thế nhóm - OH khi đun sôi Axit cacboxylic với ancol (xúc tác là H2SO4 đặc) theo phản ứng dưới đây:
R(COOH)x + R’(OH)t → Ry(COO)xyR’x + xyH2O (H2SO4, t0)
- Phản ứng tách nước
2RCOOH → (RCO)2O + H2O (P2O5)
- Phản ứng oxi hóa hoàn toàn
CxHyOz + (x + y/4 - z/2)O2 → xCO2 + y/2H2O
5. Cách nhận biết axit cacboxylic
Để nhận diện sự có mặt của loại axit này, mọi người sẽ dựa vào những đặc điểm đáng chú ý sau của nó:
- Có thể làm quỳ tím chuyển thành màu đỏ khi tiếp xúc
- Khi tác dụng với kim loại, axit cacboxylic sẽ làm giải phóng khí Hidro
- Khi axit cacboxylic tác dụng với các muối cacbonat hoặc hiđrocacbonat sẽ giải phóng khí CO2.
- HCOOH cũng có phản ứng hoá học tương tự như andehit. Đó chính là có thể tạo được kết tủa trắng khi tác dụng với các muối AgNO3/NH3…
>>>XEM THÊM: Boric acid H3BO3 99%, Mỹ, 25kg/bao
6. Điều chế axit cacboxylic như thế nào?
Hiện tại, loại axit này sẽ được điều chế theo những phương thức sau đây:
- Oxy hoá rượu etylic bằng oxy trong không khí bằng phương thức sử dụng men giấm: CH3-CH2-OH + O2 → CH3COOH + H2O
- Tổng hợp axit cacboxylic từ nguyên liệu là acetylen qua 2 phản ứng hoá học sau đây:
1, Thực hiện oxy hoá alcohol: R-CH2-OH + O2 → R-CHO + H2O
2, Tiếp tục bằng cách oxi hóa aldehyd đã thu được theo phản ứng sau: R-CHO + [O] → R-COOH
>>>XEM THÊM: Potassium carbonate K2CO3 99.5%, xuất xứ Hàn Quốc, đóng gói 25kg/bao
7. Ứng dụng của axit cacboxylic trong đời sống
Các axit cacboxylic có nhiều ứng dụng khác nhau. Nhiều axit cacboxylic được sản xuất công nghiệp trên quy mô lớn. Este của axit béo là thành phần chính của lipit và polyamit của axit aminocacboxylic là thành phần chính của protein.
Với mỗi loại acid lại được sử dụng trong các ngành công nghiệp khác nhau như sau:
- Axit formic là axit cacboxylic đơn giản nhất được sử dụng làm chất khử trùng, chất xử lý vải dệt và làm chất khử axit.
- Axit xitric được dùng làm chất điều hương vị và chất bảo quản trong thực phẩm và đồ uống.
- Axit axetic được sử dụng rộng rãi trong sản xuất nhựa xenlulose và este. Ngoài ra, nó còn giúp tạo vị chua cho giấm, giấm gia dụng chứa khoảng 5% axit axetic. Aspirin là este của axit salicylic là hoạt chất được ứng dụng rộng rãi trong công nghiệp dược phẩm được điều chế từ axit axetic.
- Axit propionic là chất bảo quản thực phẩm.
- Axit palmitic và axit stearic rất quan trọng trong sản xuất xà phòng, mỹ phẩm, dược phẩm, nến và lớp phủ bảo vệ. Ngoài ra, axit stearic cũng được sử dụng trong cao su nhân tạo.
- Axit acrylic được sử dụng như là một este trong sản xuất polyme.
- Axit metacrylic hoạt động như một este và được polyme hóa để tạo thành Lucite.
- Axit oleic được sử dụng trong sản xuất xà phòng và chất tẩy rửa và dệt may.
Ứng dụng của axit cacboxylic
8. Câu hỏi thường gặp liên quan đến axit cacboxylic
8.1. Mùi của axit này có gì đặc trưng?
Axit này có mùi chua nồng rất dễ nhận biết. Tuy nhiên, một este - biến thể của acid này lại mang mùi hương cực kỳ dễ chịu nên được dùng trong quá trình sản xuất các loại nước hoa.
8.2. Đặc điểm nhận dạng của axit cacboxylic là gì?
Phương pháp quang phổ hồng ngoại thường được dùng để nhận diện axit nỳ trong các mẫu thử. Dao động của liên kết C=O trong chất này sẽ cho ra một mũi hấp thụ nhọn ở số sóng nằm trong khoảng giữa các mức 1680 và 1725 cm−1. Nhờ vậy, việc nhận diện trở nên dễ dàng hơn rất nhiều.
8.3. Trong cuộc sống axit cacboxylic tồn tại ở dạng nào?
Trong cuộc sống thường ngày, axit cacboxylic tồn tại ở nhiều dạng khác nhau. Ví dụ cụ thể như trong thành phần cơ bản của protein, trong giấm ăn… Khi mất đi một proton H+, nhóm chức carboxyl sẽ trở thành một anion quan trọng của carboxylate.
Trên đây là những thông tin cơ bản về axit cacboxylic. Nếu có bất cứ thắc mắc nào bạn có thể liên hệ với chúng tôi qua số hotline 0826 010 010 hoặc tham khảo thêm những bài viết trên vietchem.com.vn.



















![Ảnh Anime Cute Phô Mai Que Đẹp [102+ Hình Siêu Cute]](/uploads/blog/2024/11/25/abe5e97926c8d9f39bb0d04c91c956cbbc32fbca-1732503618.jpg)

