Anilin là chất gì? Anilin có tan trong nước không? Phân biệt với phenol
Anilin là hợp chất hữu cơ, thuộc dãy đồng đẳng amin có công thức hoá học là C6H5NH2, có nhiều ứng dụng trong tổng hợp hoá học, sản xuất thuốc nhuộm, chế biến cao su,... Anilin có công thức là gì? Có làm đổi màu quỳ tím hay không? Anilin có tan trong nước không? Chúng ta cùng tìm lời giải đáp qua bài viết dưới đây.
1. Anilin là chất gì?
- Anilin là tên gọi bắt nguồn từ tiếng pháp aniline /anilin, thuộc dãy đồng đẳng amin.
- Các tên gọi khác: Phenylamin, Aminobenzen, Benzenamin.
- Anilin có công thức là C6H7N hay C6H5NH2. Đây là hợp chất amin thơm có cấu tạo đơn giản.
- Hoá chất này có mùi khó chịu giống với mùi cá ươn, ít tan trong nước, dễ dàng tan trong cồn, xăng, dầu ăn. Anilin cũng dễ cháy tạo ra khói.
- Nó được ứng dụng phổ biến trong sản xuất poly ure.
2. Cấu tạo Anilin
Anilin được cấu tạo từ gốc phenyl liên kết với nhóm chức amin.
Anilin là một phân tử hơi có cấu trúc hình tháp, trong đó nitơ nằm ở một vị trí đâu đó giữa sp3 và sp2. Do đó, cặp nitơ đơn độc ở trong một orbital lai hóa sp x với tính chất p cao. Nhóm amino trong anilin có cấu trúc phẳng hơn so với nhóm amino trong amin béo, điều này là do sự liên hợp của cặp electron tự do với nhóm thế aryl.
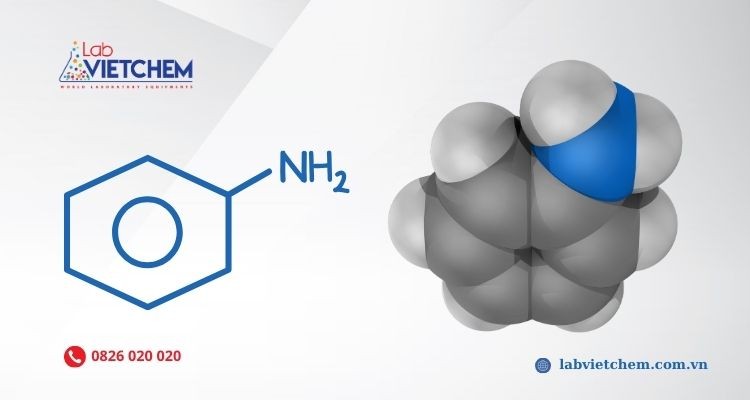
Hình 1: Cấu tạo Anilin
3. Các tính chất đặc trưng của Anilin
3.1. Tính chất vật lý
Tính chất
Đặc điểm
Bề ngoài
Tồn tại dưới dạng chất lỏng, không màu
Mùi vị
Mùi khó chịu, xốc, giống với mùi cá ươn
Khối lượng mol
93,13 g/mol
Tỷ trọng
1,0217 g/ml
Nhiệt độ nóng chảy
-6,3 độ C
Nhiệt độ sôi
184,13 °C
Độ hoà tan
- Ít tan trong nước: Tại 20 độ C độ hoà tan là 3,6 g/100 ml .
- Tan tốt trong ethanol, aceton.
Hằng số axit (pKa)
4,87
Hằng số base (pKb)
9,42
Độ nhớt
Tại 25 độ C: 3,71

Hình 2: Hóa chất Anilin
3.2. Tính chất hoá học
- Phản ứng oxi hóa: Khi tiếp xúc với không khí, Anilin sẽ xảy ra quá trình oxi hóa chậm tạo thành các vết sậm màu nâu đen.
- Tính kiềm: Anilin là một base yếu. Các hợp chất amin như anilin có tính kiềm yếu hơn so với amoniac. Anilin gần như không tan trong nước, nhưng có thể hòa tan trong nước sôi.
- Tính chất của vòng benzen: Do có nhóm -NH2, mật độ electron trong vòng benzen của anilin cao hơn so với benzen. Vì thế, trong phản ứng thế, vị trí ortho và para (liên quan đến nhóm -NH2) được ưu tiên và phản ứng diễn ra dễ dàng hơn.
C6H5NH2 + 3Br2 → C6H2Br3NH2 (↓ trắng) + 3HBr
3 nguyên tử Brom thế vào 3 nguyên tử H ở vị trí ortho và para do ảnh hưởng của nhóm NH2.
- Tính chất của nhóm amin: Anilin tác dụng với acid nitric ở nhiệt độ thấp (0-5 độ C), tạo ra các hợp chất diazoni:
C6H5NH2 + HONO → C6H5N2+Cl- + 2H2O
Các hợp chất diazoni sau đó được sử dụng làm tiền chất để sản xuất thuốc nhuộm azo. Do đó, anilin được sản xuất với số lượng lớn để dùng làm nguyên liệu cho các loại thuốc nhuộm khác.
- Anilin cũng có khả năng phản ứng với các rượu. Quá trình này được gọi là phản ứng Friedel-Craft.
C6H5NH2 + 2CH3OH → C6H5N(CH3)2 + 2H2O
C6H5NH2 + CH3OH → C6H5NHCH3 + H2O
Anilin cũng có thể tác dụng trực tiếp với các dẫn xuất halogen, tạo thành các hợp chất amin bậc hai hoặc ba. Sau đó, NaOH/KOH được sử dụng để tách acid halogenic ra khỏi hỗn hợp.
4.Tổng hợp phương pháp điều chế Anilin
Anilin được tổng hợp qua từng giai đoạn sau:
- Giai đoạn 1: Nitrat hoá benzen bằng axit nitric trong môi trường axit sunfuric ở nhiệt độ 50-60 độ C: Sản phẩm thu được là nitrobenzen, phản ứng này kèm theo toả nhiệt mạnh, có thể gây nổ:
C6H6 + HNO3 → C6H5NO2 + H20
- Giai đoạn 2: Thực hiện phản ứng cộng hydro với tác nhân xúc tác là kim loại nhóm 10 như Ni, Platin, palladium,...
C6H5NO2 + H2 → C6H5NH2 + H20
Ngoài ra, anilin có thể được tổng hợp từ amoniac và phenol có nguồn gốc từ cumen.
5. Những ứng dụng nổi bật về Anilin
5.1. Ngành dệt nhuộm
Anilin là nguồn nguyên liệu chính để sản xuất ra các loại thuốc nhuộm tổng hợp thông qua hợp chất diazoni. Nó giúp nhuộm sợi vải, da hoặc giấy.

Hình 3: Anilin là nguyên liệu trong sản xuất thuốc nhuộm dùng trong ngành dệt nhuộm
5.2. Tổng hợp hoá học
Anilin tham gia vào quá trình tổng hợp metylendianilin, 4,4′-Methylenedianiline ( MDA ) và nhiều hợp chất khác nữa.
Bên cạnh đó, nó còn tham gia vào sản xuất polyme, chế biến cao su và dược phẩm,...
6. Giải đáp thắc mắc một vài câu hỏi về Alinin
6.1. Anilin có làm đổi màu quỳ tím không?
Anilin được biết đến là hợp chất hữu cơ có tính kiềm yếu . Về bản chất, base sẽ làm quỳ tím hoá xanh. Truy nhiêu anilin có tính bazơ rất yếu, dung dịch của nó không làm thay đổi màu của giấy quỳ.
6.2. Anilin có tan trong nước không?
Câu trả lời là có. Anilin tan được trong nước nhưng rất ít. Tại 20 độ C, độ hòa tan của nó trong nước chỉ ở mức 3,6g/100ml.
Trong điều kiện nước đun sôi thì khả năng hoà tan của anilin sẽ tốt hơn.
6.3. Anilin có độc không?
Theo phân loại của EU thì C6H5NH2 được xếp vào chất gây độc, có mùi xốc.
Trong quá trình thao tác, nếu dính phải lên da sẽ gây ra tình trạng bỏng rát.
Nếu hít phải có thể gây ra tình trạng đau đầu, buồn nôn, chóng mặt,...
Ngoài ra, chất này cũng thể gây cháy khi tiếp xúc với các tác nhân khác.
7. Địa chỉ mua hoá chất Anilin chính hãng, giá tốt?
Anilin là hoá chất được ứng dụng rộng rãi trong ngành dệt nhuộm và tổng hợp hoá học nên nhu cầu sử dụng tương đối cao. Nếu quý khách hàng không biết mua hoá chất Anilin ở đâu uy tín, chất lượng thì hãy lựa chọn LabVIETCHEM - một trong những đơn vị hàng đầu trong lĩnh vực cung ứng hoá chất, thiết bị, dụng cụ phòng thí nghiệm. Chúng tôi cung cấp đa dạng hàng ngàn sản phẩm đến từ hơn 100 thương hiệu nổi tiếng khác nhau trên thế giới. Cam kết hàng chính hãng, đảm bảo chất lượng, có đủ hoá đơn chứng từ. Bên cạnh đó, dịch vụ giao hàng nhanh chóng, đội ngũ chuyên viên tư vấn nhiệt tình.
Nếu quý khách hàng muốn mua sản phẩm hãy liên hệ ngay tới số hotline 0826 020 020 để được tư vấn miễn phí và báo giá nhanh chóng.
Link nội dung: https://getairvestal.com/anilin-la-chat-gi-anilin-co-tan-trong-nuoc-khong-phan-biet-voi-phenol-a14609.html