Tìm hiểu: Tính chất hoá học của HCl, HCl có độc không?
Với lượng sản xuất lên tới 20 triệu tấn mỗi năm, axit clohidric là một nguồn nguyên liệu khá phổ biến và có tính ứng dụng cao đối với con người. Tuy nhiên mang đặc tính của một axit mạnh, đây vẫn là một hoá chất gây độc. Vậy tính chất hoá học của HCl là gì? Cần lưu ý những gì khi sử dụng một axit có tính độc? Hãy cùng Hanteco đi tìm hiểu qua bài viết dưới đây nhé!
HCl là gì?
Axit clohiđric hay còn gọi là axit muriatic… (ký hiệu hoá học: HCl). Khi ở thể khí, axit HCl không màu, mùi xốc, nặng hơn không khí và tan nhiều trong nước tạo thành dung dịch HCl có tính axit mạnh.
Khi ở thể lỏng, axit HCl là một dung dịch loãng không màu, có khả năng bay hơi, nhưng không dễ cháy.
 Dung dịch Axit clohiđric
Dung dịch Axit clohiđric
Nồng độ tối đa của axit HCl đậm đặc là 40%, lúc này dung dịch có màu hơi ngả vàng. Có khả năng tạo thành các sương mù axit trong môi trường không khí ẩm.
Tính chất hoá học của HCl
Tính chất hoá học của HCl bao gồm các đặc tính của một axit mạnh như:
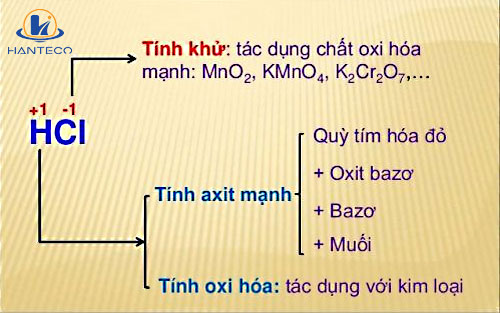 HCl có tính chất hóa học đặc trưng của một axit
HCl có tính chất hóa học đặc trưng của một axit
- Axit HCl làm đổi màu quỳ tím: Khi nhúng quỳ tím vào dung dịch axit sẽ có hiện tượng quỳ tím chuyển đỏ.
- Axit clohidric tác dụng với kim loại đứng trước H, tạo thành muối và hidro
Fe + 2HCl → FeCl2 + H2↑
- Axit clohidric tác dụng với oxit kim loại, tạo thành muối Clorua và nước
6HCl + Al2O3 →2AlCl3 + 3H2O
- Axit clohidric tác dụng với Bazơ, tạo thành muối Clorua và nước
3HCl + Al(OH)3 → AlCl3 + 3H2O
- Axit clohidric tác dụng với muối, tạo thành muối mới và axit mới
AgNO3 + 2HCl → AgCl↓ + HNO3
- Axit clohidric tác dụng với hợp chất có tính oxi hoá, thể hiện tính khử
6HCl + KClO3 → KCl + 3Cl2↑ + 3H2O
Lưu ý: Axit HCl sẽ không tác dụng với những kim loại đứng sau H trong dãy điện hoá, không tác dụng với các phi kim, axit, oxit kim loại, oxit phi kim.
Điều chế và sản xuất axit HCl
Điều chế HCl trong phòng thí nghiệm
Trong phòng thí nghiệm, dựa vào tính chất hoá học HCl được điều chế bằng phương pháp đun nóng muối NaCl thể rắn với axit H2SO4 đặc.
NaCl (rắn) + H2SO4 đặc → NaHSO4 + HCl
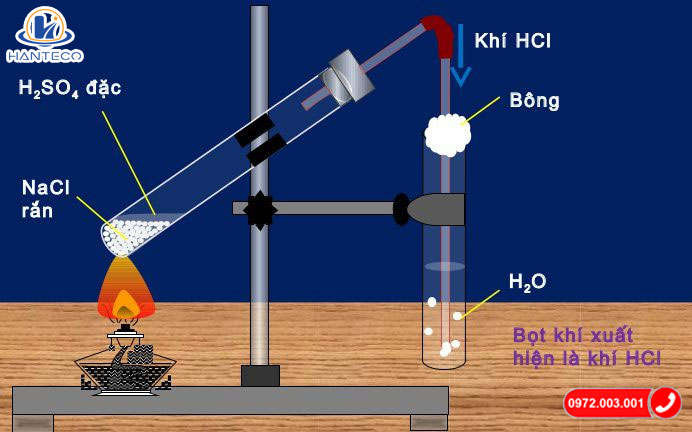 Mô phỏng thí nhiệm điều chế HCl trong phòng thí nghiệm
Mô phỏng thí nhiệm điều chế HCl trong phòng thí nghiệm
Sản phẩm thu được là HCl với độ tinh khiết cao, có thể đạt tới nồng độ 40%
Sản xuất HCl trong công nghiệp
Phục vụ cho mục đích thương mại, người ta chủ yếu sản xuất axit HCl bằng cách tổng hợp trực tiếp hai khí là Clo và Hidro. Sau khi tổng hợp hỗn hợp khí này sẽ dùng nước sạch để hấp thụ và thu lại dung dịch Axit Clohidric:
H2 + Cl2 →2HCl
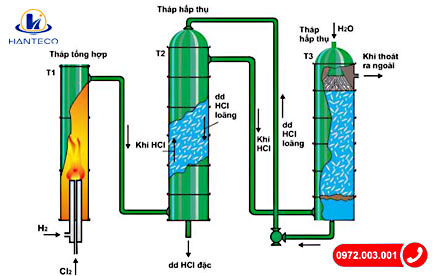 Điều chế axit Axit clohiđric trong công nghiệp
Điều chế axit Axit clohiđric trong công nghiệp
Những ứng dụng dựa trên tính chất hoá học của HCl
Tính chất hoá học HCl có những đặc trưng cơ bản của một axit mạnh, vì vậy đây là một dung dịch axit có tính ứng dụng cao trong cuộc sống. Sau đây là một phải ứng dụng tiêu biểu phải kể đến của axit clohidric:
 Những ứng dụng phổ biến của Axit clohiđric
Những ứng dụng phổ biến của Axit clohiđric
- Tẩy gỉ bề mặt kim loại: Tiếp xúc với môi trường sau một thời gian thì các kim loại như sắt, thép…sẽ có hiện tượng han gỉ vì bị oxi hoá. Để khắc phục tình trạng này, ta có thể sử dụng HCl với nồng độ 18% để lấy lại một bề mặt sáng bóng như mới cho kim loại.
- Sản xuất hợp chất hữu cơ: axit HCl có thể dùng trong việc sản xuất ra Vinyl clorua, dicloetan - thành phần chính của nhựa PVC, hay than hoạt tính.
- Sản xuất hợp chất vô cơ: axit HCl là một trong những thành phần chính tạo nên các hóa chất PAC trợ lắng, các loại vật liệu để mạ điện như muối canxi clorua, niken (II) clorua. Đây là những nguyên liệu chủ yếu để sử dụng làm chất keo tụ dùng cho xử lý nước thải, sản xuất giấy…
- Cân bằng độ PH: Khi nước bể bơi có nồng độ PH cao vượt ngưỡng 7,6 thì ta có thể sử dụng HCl như là một hóa chất xử lý nước giúp làm giảm độ PH về mức cân bằng.
 Axit clohiđric có công dụng làm giảm nồng độ PH trong nước
Axit clohiđric có công dụng làm giảm nồng độ PH trong nước
- Các ứng dụng khác: Axit HCl còn được ứng dụng trong ngành công nghiệp khai thác dầu, khử axit trong các thực phẩm đóng hộp cho thời gian bảo quản được lâu hơn, vệ sinh nhà cửa…
Lưu ý trong quá trình bảo quản và sử dụng HCl
Tính chất hoá học của HCl cho biết rằng đây là một hợp chất độc, có thể gây ra những tác hại đối với sức khỏe con người. Chính vì vậy, trong quá trình bảo quản, sử dụng hoá chất này, ta cần đặc biệt lưu ý những điều sau:
 Tránh tiếp xúc trực tiếp với hóa chất Axit clohiđric
Tránh tiếp xúc trực tiếp với hóa chất Axit clohiđric
Trong bảo quản
- Sử dụng những vật liệu chứa đựng chống được sự ăn mòn của axit.
- Không để gần những chất dễ cháy nổ, chất có tính oxi hoá.
- Để hóa chất nơi thoáng mát, tránh nước và ánh nắng trực tiếp của mặt trời.
Khi sử dụng
- Cần trang bị đầy đủ những thiết bị bảo hộ, tránh tiếp xúc trực tiếp với hoá chất.
- Dùng nước để xử lý, xả sạch trong trường hợp axit bị rơi vãi ra ngoài hay bắn vào cơ thể. - Kiểm tra nồng độ các thành phần trong nước thường xuyên. Không sử dụng nước hồ bơi ngay sau khi vừa châm hóa chất xử lý.
Địa chỉ bán hóa chất HCl giá tốt
Hanteco hiện đang là một trong những đơn vị cung cấp hóa chất HCl 32% uy tín, giá tốt nhất thị trường.
Dung dịch Axit clohiđric 32% xử lý nước hồ bơi hiệu quả
Những sản phẩm hóa chất xử lý nước bể bơi do Hanteco cung cấp luôn đảm bảo là hàng chính hãng, đầy đủ giấy tờ CO, CQ và chất lượng vượt trội. Để được tư vấn hỗ trợ mua hóa chất HCL và các thiết bị hồ bơi, hóa chất khác với giá hấp dẫn xin quý khách vui lòng liên hệ tới số hotline 0972.003.001 (miền Bắc) và 0986.365.003 (miền Nam).
Link nội dung: https://getairvestal.com/tim-hieu-tinh-chat-hoa-hoc-cua-hcl-hcl-co-doc-khong-a14711.html